
34. Selen (Se) <— 35. Brom (Br) —> 36. Krypton (Kr)
https://sv.wikipedia.org/wiki/Brom
https://en.wikipedia.org/wiki/Bromine
Generella egenskaper
Relativ atommassa: 79,904
Utseende: Rödbrun ångande vätska
Fysikaliska egenskaper
Densitet (vid rumstemperatur): 3.1028 g/cm3
Aggregationstillstånd: Flytande
Smältpunkt: 265,8 K (−7 °C)
Kokpunkt: 332 K (59 °C)
Trippelpunkt: 265,90 K, 5,8 kPa
Molvolym: 19,78 × 10−6 m3/mol
Smältvärme: 5,286 kJ/mol
Ångbildningsvärme: 15,438 kJ/mol
Molär värmekapacitet: 75,69 J/(mol·K)
Atomära egenskaper
Atomradie: 115 (94) pm
Kovalent radie: 114 pm
van der Waalsradie: 185 pm
Elektronkonfiguration
Elektronkonfiguration: [Ar] 3d10 4s2 4p5
e− per skal: 2, 8, 18, 7
Kemiska egenskaper
Oxidationstillstånd: −1, +1, +3, +4, +5, +7
Oxider (basicitet): Starkt sur
Elektronegativitet (Paulingskalan): 2,96
Diverse
Kristallstruktur: Ortorombisk
Ljudhastighet: 206 m/s (at 20 °C)
Värmeledningsförmåga: 0,122 W/(m⋅K)
Elektrisk resistivitet: 7.8×1010 Ω⋅m (at 20 °C)
Magnetism: Diamagnetisk
Magnetisk susceptibilitet: −56.4×10−6 cm3/mol
Identifikation
CAS-nummer: 7726-95-6
Historia
Namnursprung:
Förutsägelse:
Upptäckt och första isolation:
Isotoper
| Isotop | Förekomst | Halveringstid (t1/2) | Sönderfall | Sönderfallsprodukt |
|---|---|---|---|---|
| 79Br | 51% | Stabil | ||
| 81Br | 49% | Stabil |
https://en.wikipedia.org/wiki/Isotopes_of_bromine
Brom
Brom (latinskt namn, bromum) är ett icke-metalliskt grundämne som tillhör gruppen halogener.
Historia
Brom upptäcktes 1826 av fransmannen Antoine Jérôme Balard i moderluten från havssaltstillverkning. Bromets existens verifierades av Gay-Lussac och Thénard, samt Vauquelin. Gay-Lussac föreslog namnet brom, som hämtats från grekiskans bronos, stank, och syftar på bromets starka lukt. Oberoende av Barnard utvanns brom vid samma tid av tyskarna Carl Jacob Löwig och Justus von Liebig.
Egenskaper
Vid standardtryck och -temperatur är brom en mörk rödbrun frätande vätska, som avger giftiga ångor med obehaglig lukt. Brom löst i vatten kallat bromvatten är ett reagens på omättade kolväten. De reagerar och bryter sina dubbelbindningar och binder in bromatomerna och det brunfärgade bromvattnet förlorar färgen.
Användningsområde
Flamskyddsmedel
Brom används som komponent i en mängd olika sammansättningar flamskyddsmedel som gemensamt kallas bromerade flamskyddsmedel. De används för att förhindra brand och i nästa steg fördröja och minimera spridningen av brandförloppet och är vanligt förekommande i fordonsinredning samt elektronisk utrustning som datorer, tv-apparater och kontorsmaskiner. Bromerade flamskyddsmedel är skadliga för miljö och hälsa.[2]
Fotopapper
Brom i förening med silver, silverbromid (AgBr), används tack vare sin ljuskänslighet vid tillverkning av fotopapper.
Medicin
Från 1850-talet och till början av 1900-talet var alkalibromider, särskilt kaliumbromid, vanligt använda inom sjukvården på grund av sin sedativa verkan. På grund av bromidens toxicitet och bieffekter, som kallas bromism, upphörde användningen. I vissa länder förekommer fortfarande en begränsad användning av kaliumbromid i kombination med fenobarbital mot epilepsi, och ämnet förekommer även inom veterinärmedicinen.
Farliga egenskaper
Brom orsakar vid hudkontakt frätskador som kan bli djupa och svårläkta. Förtäring eller inandning orsakar förgiftning som kan vara livshotande.
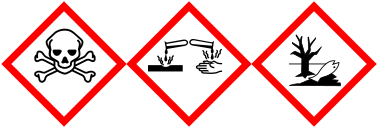
| H-fraser | H303, H314, H330, H400 |
|---|---|
| P-fraser | P260, P273, P280, P284, P305 + P351 + P338, P310 |
http://www.periodicvideos.com/

Speak Your Mind